علامات وأعراض مرض جريفز من ويكيبيديا، الموسوعة الحرة
تنجم علامات مرض جريفز( Graves' disease) وأعراضه بشكل عام عن التأثيرات المباشرة وغير المباشرة لفرط نشاط الغدة الدرقية ، باستثناء حالات اعتلال العين لدى غريفز ، وتضخم الغدة الدرقية والوذمة المخاطية القبيحة (التي تسببها عمليات المناعة الذاتية لمرض جريفز). هذه المظاهر السريرية دراماتيكية وتنطوي على كل جهاز في الجسم. الآليات التي تتوسط هذه الآثار ليست مفهومة جيدًا. ترتبط شدة علامات وأعراض فرط نشاط الغدة الدرقية بمدة المرض ، وحجم هرمون الغدة الدرقية الزائد ، وعمر المريض. هناك أيضًا تنوع كبير في الاستجابة الفردية لفرط نشاط الغدة الدرقية والحساسية الفردية لتقلبات هرمون الغدة الدرقية بشكل عام. علاوة على ذلك ، يمكن لمرضى مرض جريفز الخضوع لفترات من قصور الغدة الدرقية (لمزيد من المعلومات ، انظر أعراض قصور الغدة الدرقية): قد يكون العثور على الجرعة المناسبة من كبت هرمون الغدة الدرقية و / أو المكملات أمرًا صعبًا ويستغرق وقتًا. يمكن أن تتغير أيضًا حاجة الجسم لهرمون الغدة الدرقية بمرور الوقت ، كما هو الحال في الأشهر الأولى بعد العلاج باليود المشع (RAI). يمكن أن تكون أمراض المناعة الذاتية في الغدة الدرقية متقلبة أيضًا: فرط نشاط الغدة الدرقية يمكن أن يتقاطع مع قصور الغدة الدرقية والغدة الدرقية.
عام
تضخم الغدة الدرقية (تضخم الغدة الدرقية). إذا نمت الغدة الدرقية بشكل كبير بما فيه الكفاية ، فقد تضغط على العصب الحنجري الراجع ، مما يؤدي إلى شلل الحبل الصوتي ، وخلل الصوت ، وحتى صرير التنفس. قد يؤدي ضغط السلسلة المتعاطفة إلى متلازمة هورنر .
اعتلال العين في جريفز (بروز إحدى العينين أو كلتيهما)
وذمة مخاطية قبل الحكة
قد تشمل ميزات القلب والأوعية الدموية ارتفاع ضغط الدم ومعدل ضربات القلب التي قد تكون سريعة أو غير منتظمة في طبيعتها ؛ قد يُنظر إليها على أنها خفقان .
تشمل النتائج الأقل شيوعًا تضخم البطين الأيسر ، وتقلصات الأذين البطيني وأوانها ، والرجفان الأذيني ، وفشل القلب الاحتقاني ، والذبحة الصدرية ، واحتشاء عضلة القلب ، والانصمام الجهازي ، والوفاة من انهيار القلب والأوعية الدموية ومقاومة بعض الآثار الدوائية ( ديجوكسين ، كومادين ).
فرط المنعكسات ، مع مرحلة استرخاء سريعة.
رد فعل مفرط بشكل واضح لجميع أنواع المحفزات.
غالبًا ما تكون الزيادة الملحوظة في التعب ، أو الوهن ، بارزة. يمكن الجمع بين هذا التعب المتزايد مع فرط النشاط . يلاحظ المرضى أنهم مضطرون إلى النشاط المتواصل ، والذي يتسبب في إرهاق كبير.
أرق رعاش (اهتزاز ناعم عادة ، رعاش أصابع ممدودة). في دراسة صغيرة لمرضى فرط نشاط الغدة الدرقية المشخصين حديثًا ، لوحظ رعاش في 76٪ منهم. تضع بعض الدراسات سبب ارتعاش الغدة الدرقية مع ارتفاع حالة بيتا الأدرينالية ، وتشير دراسات أخرى إلى زيادة التمثيل الغذائي للدوبامين . فقدان الوزن على الرغم من الشهية الطبيعية أو المتزايدة. يزداد وزن بعض المرضى (خاصة الأصغر منهم) بسبب التحفيز المفرط للشهية الذي يتجاوز تأثير فقدان الوزن.
زيادة الشهيه .
ضعف أو ضعف العضلات (خاصة في عضلات الذراعين والساقين الكبيرة). يحدث هذا الأخير في 60 إلى 80 في المائة من المرضى الذين يعانون من فرط نشاط الغدة الدرقية غير المعالج.
نادرا ما يكون ضعف العضلات هو الشكوى الرئيسية. ترتبط احتمالية ودرجة ضعف العضلات مع مدة وشدة حالة فرط نشاط الغدة الدرقية ، وتصبح أكثر احتمالية بعد سن الأربعين. تعود قوة العضلات تدريجيًا على مدار عدة أشهر بعد علاج فرط نشاط الغدة الدرقية.
تنكس العضلات
ضيق التنفس
زيادة التعرق
عدم تحمل الحرارة
جلد دافئ ورطب
شعر رقيق وناعم
احمرار المرفقين موجود بشكل متكرر. من المحتمل أن يكون نتيجة لمزيج من زيادة النشاط ، جزء مكشوف ، ونظام حركي وعائي مفرط التهيج.
التهابات الجيوب الأنفية المزمنة
أظافر هشة
مسمار بلامر
تضخم الثدي غير الطبيعي عند الرجال
أعراض الجهاز الهضمي. يشمل ذلك زيادة حركات الأمعاء ، لكن سوء الامتصاص غير معتاد.
زيادة مستويات الكالسيوم في الدم (بنسبة تصل إلى 25 ٪ - تعرف باسم فرط كالسيوم الدم ). يمكن أن يسبب هذا اضطراب في المعدة ، والتبول المفرط ، وضعف وظائف الكلى.
يمكن تنشيط مرض السكري أو تكثيفه وتفاقم سيطرته. يتم تحسين مرض السكري أو قد يختفي عند علاج التسمم الدرقي.
يمكن العثور على دليل على مرض كبدي خفيف أو شديد.
قد تشمل الأعراض التناسلية لدى الرجال انخفاض هرمون التستوستيرون الحر (بسبب ارتفاع مستوى الجلوبيولين المرتبط بهرمون التستوستيرون) ، تناقص الرغبة الجنسية ، ضعف الانتصاب وضعف (عكسى) إنتاج الحيوانات المنوية مع انخفاض متوسط كثافة الحيوانات المنوية ، ارتفاع معدل حدوث تشوهات الحيوانات المنوية ، وانخفاض حركة الخلايا المنوية. قد تواجه النساء الحيض نادرة أو غير النظامية ويذكر تدفق الطمث جنبا إلى جنب مع تصور صعوبة، العقم والمتكررة الإجهاض . قد تحدث نوبات عصبية ، اعتلال عصبي من انحباس العصب عن طريق آفات الوذمة المخاطية قبل الحكة ، والشلل الدوري لنقص بوتاسيوم الدم . كنعاني ، choreia ، و الضرر الجهاز القشري ، نادرة. يعتبر الاعتلال الدماغي الحاد للدماغ نادرًا جدًا.
التأثيرات على الهيكل العظمي
ويرتبط فرط نشاط الغدة الدرقية الصريح بإعادة تشكيل العظام المتسارع (مما يؤدي إلى زيادة مسامية العظام القشرية وانخفاض حجم العظام الترابية) ، وانخفاض كثافة العظام بشكل عام ، وهشاشة العظام ، وزيادة في معدل الكسر. ترتبط التغيرات في التمثيل الغذائي للعظام بتوازن الكالسيوم السلبي ، وزيادة إفراز الكالسيوم والفوسفور في البول (فرط كالسيوم البول) والبراز ، ونادراً فرط كالسيوم الدم. في فرط نشاط الغدة الدرقية ، تنخفض مدة الدورة الطبيعية لارتشاف العظام لمدة 200 يومًا تقريبًا ، وترتبط كل دورة بفقدان العظام بنسبة 9.6 بالمائة. في قصور الغدة الدرقية ، تقرب مدة الدورة 700 يوم تقريبًا وترتبط بزيادة بنسبة 17 بالمائة في العظم المعدني.
مدى انخفاض كثافة العظام في معظم الدراسات هو 10-20٪. تختلف المظاهر السريرية على العظام اعتمادًا على عمر المريض. المرأة بعد سن اليأس هي الأكثر حساسية لفقدان العظام المتسارع من التسمم الدرقي. يمكن أن يؤدي نمو العظام المتسارع لدى الأطفال المتناميين إلى زيادة التعظم على المدى القصير ، ولكنه يؤدي بشكل عام إلى البالغين قصر القامة مقارنة بالارتفاعات المتوقعة.
مع إدخال الأدوية المضادة للغدة الدرقية واليود المشع في أربعينيات القرن الماضي ، أصبح مرض عظم فرط نشاط الغدة الدرقية الظاهر سريريًا أقل شيوعًا. ومع ذلك ، فقد أظهرت قياسات كثافة العظام أن فقدان العظام شائع في المرضى الذين يعانون من فرط نشاط الغدة الدرقية ، وبدرجة أقل ، في المرضى الذين يعانون من فرط نشاط الغدة الدرقية تحت السريري. إن تاريخ فرط نشاط الغدة الدرقية هو عامل خطر لكسر الورك في وقت لاحق من الحياة ، والذي بدوره هو أحد أسباب الوفاة المتأخرة الزائدة في مرضى فرط نشاط الغدة الدرقية سابقًا. لذلك من المنطقي الافتراض أنه في بعض مرضى فرط نشاط الغدة الدرقية ، لا تعود كثافة العظام تمامًا إلى وضعها الطبيعي بعد العلاج المضاد للغدة الدرقية.
ومع ذلك ، إذا تم علاج التسمم الدرقي مبكرًا ، يمكن تقليل فقدان العظام. يمكن تحديد مستوى الكالسيوم في الدم عن طريق اختبار دم بسيط ، ويمكن لفحص كثافة العظام توثيق كمية فقدان العظام. هناك العديد من الأدوية التي يمكن أن تساعد في إعادة بناء كتلة العظام ومنع المزيد من فقدان العظام. وقد ثبت أن العلاج Risedronate للمساعدة في استعادة كتلة العظام في هشاشة العظام / هشاشة العظام المرتبطة بمرض جريفز. ومع ذلك ، فإن تمارين تحمل الوزن ، واتباع نظام غذائي متوازن ، واستهلاك الكالسيوم من حوالي 1500 ملغ في اليوم وما يكفي من فيتامين د ، هي بالطبع أسس أولية.
=====
علامات وأعراض التصلب المتعدد من ويكيبيديا، الموسوعة الحرة
يمكن أن يسبب التصلب المتعدد مجموعة متنوعة من الأعراض، منها: تغيرات في الإحساس (نقص الحس)، ضعف العضلات، تشنجات عضلية غير طبيعية، أو صعوبة في الحركة؛ صعوبات في التنسيق والتوازن، مشاكل في الكلام (رتة) أو البلع (عسر البلع)، مشاكل بصرية (رأرأة، التهاب العصب البصري، ازدواج الرؤية)، التعب ومتلازمة الآلام الحادة أو المزمنة، ضعف الإدراك، أو أعراض العاطفية (الاكتئاب الشديد بشكل رئيسي). المقياس السريري الرئيسي المُعتمد في قياس تطور درجة الإعاقة وشدة الأعراض (إي دي إس إس).غالبًا ما تكون الهجمات الأولية عابرة وخفيفة (أو بدون أعراض) ومحددة لذاتها، ولا تتطلب زيارة أماكن الرعاية الصحية وأحيانًا لا يُوضع التشخيص إلا بعد حدوث مزيد من الهجمات. الأعراض الأولية الأكثر شيوعًا التي أُبلغ عنها هي: التغيرات في الإحساس في الذراعين أو الساقين أو الوجه (33%)، فقدان الرؤية الكامل أو الجزئي (التهاب العصب البصري) (20%)، الضعف (13%)، الرؤية المزدوجة (7%)، عدم الثبات أثناء المشي (5%)، ومشاكل في التوازن (3%)، ولكن أُبلغ عن العديد من الأعراض الأولية النادرة، مثل: فقدان القدرة على الكلام أو الإصابة بالذهان. يعاني 15% من الأفراد من مجموعة أعراض متعددة عندما يطلبون الرعاية الطبية لأول مرة.
المثانة والأمعاءتظهر مشاكل متعلقة بالمثانة عند 70-80% من الأشخاص المصابين بالتصلب المتعدد، ولها تأثير مهم على عادات النظافة والنشاط الاجتماعي. عادةً ما ترتبط مشاكل المثانة بمستويات عالية من الإعاقة وظهور علامات عصبية هرمية في الأطراف السفلية.المشاكل الأكثر شيوعًا هي الإلحاح البولي (سلس البول) ولكن تظهر أيضًا صعوبات في بدء التبول،
والتردد، والإحساس بعدم اكتمال عملية التبول، والاحتباس. عندما يحدث احتباس البول تصبح التهابات المسالك البولية الثانوية شائعة الحدوث.
أهداف العلاج هي التخفيف من أعراض الجهاز البولي، وعلاج التهابات المسالك البولية، وتقليل المضاعفات المحتملة، والحفاظ على وظائف الكلية. يمكن تصنيف العلاجات إلى نوعين فرعيين رئيسيين: العلاج الدوائي وغير الدوائي. تختلف العلاجات الدوائية بشكل كبير اعتمادًا على أصل الخلل الوظيفي أو نوعه وبعض الأمثلة على الأدوية المستخدمة هي: الفوزوزين للاحتباس البولي، فلافوكسات وتروسبيوم للإلحاح وسلس البول، وديسموبريسين للتبول الليلي. تتضمن العلاجات غير الدوائية ممارسة تمارين عضلات قاع الحوض، والتحفيز، وأحيانًا وضع القسطرة المثانية بشكل متقطع.تؤثر مشاكل الأمعاء على نحو 70% من المرضى، إذ يعاني نحو 50% من المرضى من الإمساك وما يصل إلى 30% من السلس الغائطي. عادةً ما يكون سبب ضعف الأمعاء لدى مرضى التصلب المتعدد إما نقص حركية الأمعاء أو ضعف التحكم العصبي في عملية التغوط. ويرتبط النوع الأول بشكل شائع بعدم القدرة على الحركة أو الآثار الثانوية للأدوية المستخدمة في علاج المرض. يمكن تخفيف الألم أو مشاكل التغوط من خلال تغيير النظام الغذائي الذي يشمل، من بين تغييرات أخرى، زيادة تناول السوائل والملينات الفموية أو التحاميل والحقن الشرجية عندما لا تكون العادات والتدابير الفموية كافية للسيطرة على المشاكل.
عاطفيًا
الأعراض العاطفية شائعة أيضًا ويُعتقد أنها استجابة طبيعية للإصابة بمرض مُوهن ونتيجة لتلف مناطق معينة من الجهاز العصبي المركزي التي تولد المشاعر وتتحكم فيها.
الاكتئاب السريري هو أكثر الحالات العصبية والنفسية شيوعًا: أُبلغ عن معدلات انتشار الاكتئاب استمر مدى الحياة بنسبة 40-50% ولمدة 12 شهرًا نحو 20% بين الأشخاص المصابين بمرض التصلب المتعدد. هذه الأرقام أعلى بكثير عند للأشخاص المصابين بأمراض مزمنة أخرى مرافقة. لقد حققت دراسات تصوير الدماغ التي تحاول ربط الاكتئاب بالآفات في مناطق معينة من الدماغ نجاحًا متغيرًا.تظهر أيضًا مشاعر أخرى لدى المرضى مثل: الغضب والقلق والإحباط واليأس المتكرر، كما أن الانتحار يمثل تهديدًا حقيقيًا فهو يؤدي إلى 15% من الوفيات عند مرضى التصلب المتعدد، نادرًا ما يظهر الذهان أيضًا.
التعب التعب شائع جدًا وأحد مسببات الإعاقة عند مرضى التصلب المتعدد وله علاقة وثيقة بأعراض الاكتئاب. عندما تبدأ معالجة الاكتئاب، فإن التعب يبدأ أيضًا بالانخفاض ويُوصى بتقييم حالة الاكتئاب عند المرضى قبل استخدام الأساليب العلاجية الأخرى. وبنفس الطريقة، يمكن أن تساهم عوامل أخرى مثل اضطراب النوم، أو الألم المزمن، أو سوء التغذية، أو حتى بعض الأدوية في الشعور بالإرهاق والتعب، ويُشجع الأطباء على تحديدها ومعالجتها. هناك أيضًا أدوية مختلفة تستخدم لعلاج التعب بالإضافة إلى التدخلات النفسية للحفاظ على الطاقة الإيجابية؛ ولكن تأثيرها ضئيل ولهذه الأسباب يُعتبر التعب من الأعراض التي يُصعب التعامل معها والسيطرة عليها. يرتبط التعب أيضًا بمناطق معينة من الدماغ عند مرض التصلب المتعدد وذلك حسب تقنيات التصوير بالرنين المغناطيسي.
تحددات الحركةتُعتبر أعراض تحدد الحركة في نشاطات مثل: المشي، والتنقلات، والتقلب في الفراش، وما إلى ذلك، شائعة لدى الأفراد الذين يعانون من التصلب المتعدد. إذ في غضون 10 سنوات بعد ظهور مرض التصلب المتعدد، يصل ثلث المرضى إلى درجة 6 على المقياس المُعتمد لتحديد درجة تطور المرض (إي دي إس إس)، ما يتطلب استخدام أداة مساعدة على المشي من جانب واحد، وبحلول 30 عامًا تزداد النسبة إلى 83%.قد توجد مجموعة كبيرة من الإعاقات لدى المصابين بمرض التصلب المتعدد والتي يمكن أن تؤثر بمفردها أو مجتمعة بشكل مباشر على توازن الشخص ووظائفه وقدرته على الحركة، وتشمل هذه الإعاقات: التعب، والضعف، وفرط التوتر، وقلة تحمل التمارين، واختلال التوازن، والرنح، والرعشة.
قد تهدف التدخلات إلى التقليل من الإعاقات الفردية التي تؤثر على الحركة، من الأمثلة على ذلك تعليم المرضى استخدام بعض المعدات مثل أدوات المساعدة على المشي والكراسي المتحركة والدراجات البخارية الآلية بالإضافة إلى تعليمات متعلقة بالاستراتيجيات التعويضية لإنجاز نشاط ما.
الألمالألم، عرض شائع عند مرضى التصلب المتعدد. تشير دراسة حديثة جمعت نتائج 28 دراسة (7101 مريضًا) بشكل منهجي إلى أن الألم يؤثر على 63% من المصابين بمرض التصلب المتعدد.
وصفت هذه الدراسات الـ 28 الألم عند مجموعة كبيرة من الأشخاص المختلفين المصابين بالتصلب المتعدد. لم يجد الباحثون أي دليل على أن الألم كان أكثر شيوعًا لدى الأشخاص في المراحل المتقدمة من المرض، أو عند الإناث مقارنة بالذكور، أو عند الأشخاص الذين يعانون من مستويات مختلفة من الإعاقة، أو عند الأشخاص الذين أصيبوا بمرض التصلب المتعدد لفترات زمنية مختلفة.
يمكن أن يكون الألم شديدًا ومنهكًا، وقد يكون له تأثير عميق على نوعية الحياة والصحة العقلية للمريض. يُعتقد أن أنواعًا معينة من الألم تظهر أحيانًا بعد إصابة السيالات الصاعدة أو الهابطة التي تتحكم في نقل المنبهات المؤلمة، ولكن توجد العديد من الأسباب الأخرى. يُعتقد أن أكثر أنواع الألم انتشارًا هو الصداع (43%) وآلام الأطراف (26%) وآلام الظهر (20%) والتشنجات المؤلمة (15%) وألم العصب ثلاثي التوائم (3%).يرجع الألم الحاد بشكل رئيسي إلى التهاب العصب البصري أو ألم العصب الثلاثي التوائم أو أو خلل الحس.
عادة ما يكون الألم تحت الحاد ثانويًا للمرض ويمكن أن يكون نتيجة لقضاء الكثير من الوقت في نفس الوضعية أو بسبب احتباس البول أو التقرحات الجلدية. الألم المزمن شائع ويصعب علاجه.
====
علاج التصلب المتعدد من ويكيبيديا، الموسوعة الحرة

صورة لشريحة مجهرية توضح أثر التصلب المتعدد في إزالة طبقة الميالين
يوجد عدد من الطرق العلاجية للتصلب المتعدد، على الرغم من عدم وجود الشفاء التام. التصلب المتعدد هو مرض التهابي مزمن مزيل لطبقة الميالين يؤثر على الجهاز العصبي المركزي. الانطباع الاولي الشائع للمرض هي حالة الانتكاسة والشفاء. تتميز هذه الفترة بالنوبات المفاجئة (الانتكاسة) متبوعة بفترة من الشفاء النسبي بدون ظهور أي علامات من النشاط المرضي. بعد عدة سنوات، العديد من الأشخاص الذين واجهوا حالة الانتكاسة ثم الشفاء يبدؤون بالمعاناة من هبوط في أداء الجهاز العصبي بدون وجود انتكاسات حادة. عندما تحدث تلك الحالة تسمى بالتصلب المتعدد المتصاعد الثانوي. النوع الآخر، وهو أقل شيوعاً، التصلب المتعدد المتصاعد الأولي (في حالة هبوط أداء الجهاز العصبي بدون نوبات مبدأية)، والتصلب المتعدد المتصاعد الانتكاسي (هبوط ثابت في أداء الجهاز العصبي مع نوبات شديدة). العديد من الطرق العلاجية تستخدم مع المرضى الذين يعانون من النوبات الحادة، سواء حالة الانتكاسة والشفاء، حالة التصلب المتعدد المتصاعد، وأيضاً في حالة المرضى الذين يعانون من زوال الميالين مع عدم تشخيصهم بالتصلب المتعدد، وأيضاً للتحكم ببعض آثار التصلب المتعدد. الهدف الأساسي من العلاج هو إعادة الوظيفة الحيوية بعد النوبات، منعاً لحدوث أخرى جديدة، ومنعً للإعاقة. وكما الحال مع أي علاج، العلاجات المستخدمة لعلاج التصلب المتعدد قد تسبب بعض الآثار الضارة، ولكن يوجد العديد من العلاجات المتاحة والتي لا تزال تحت الاختبارات.
في نفس الوقت، عدد من العلاجات البديلة تستخدم من قبل المرضى على الرغم من عدم وجود دعم أو مقارنة من قبل دراسة علمية. هذه المقالة تركز على العلاجات المستخدمة للتصلب المتعدد القياسي، لن تتطرق المقالة إلى بعض الطرق العلاجية لبعض أنواع التصلب المتعدد الغير قياسي.
النوبات الحادة
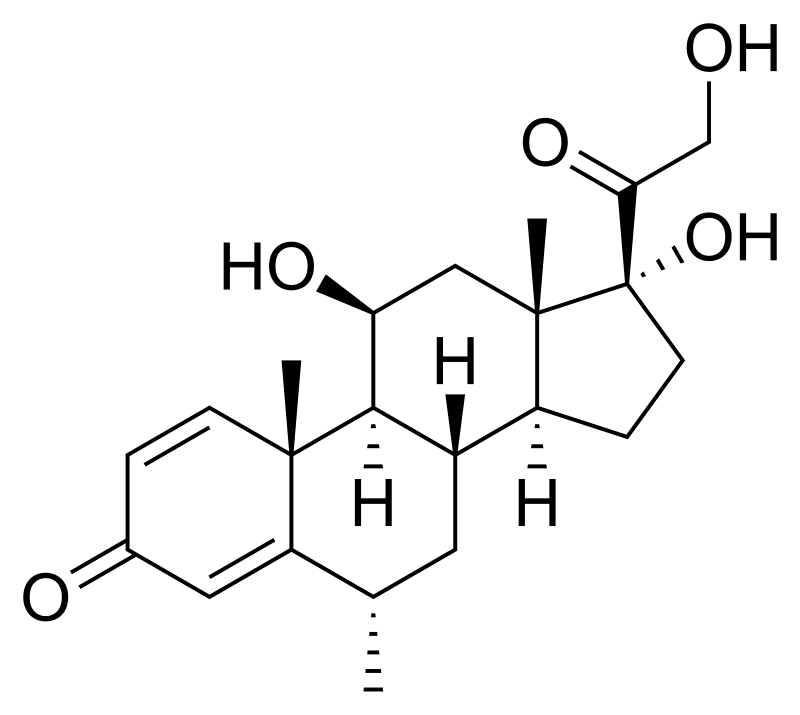
التركيب الكيميائي للميثيل بريدنيزولون. يتم استخدام الكورتيزون في حالة الانتكاسات الشديدة.
استخدام جرعات عالية من الكورتيزون الوريدي، مثل ميثيل بريدنيزولون، يعتبر علاج روتيني لعلاج الانتكاسات الحادة. يتم استخدام هذه العلاجات على مدى ثلاثة إلى خمسة أيام، ولديها فعالية عالية في تعجيل عملية الشفاء من الاعاقة بعد النوبة. عموماً، لا يوجد أدلة كافية تشير إلى تأثير إعاقي على المدى الطويل لمستخدمي علاج الكورتيزون. الستيرويدات المستخدمة عن طريق الفم تملك نفس فعالية وأمان الستيرويدات الوريدية في علاج أعراض التصلب المتعدد. في حالة النوبات الشديدة والتي لا يمكن علاجها بالكورتيزون، يتم علاجها عن طريق فصادة البلازما. الأدوية الجديدة والتي تحقن وريديا ( كالظاهرة في الأعلى ) تعطى مرة كل شهر إلى ثلاثة أشهر.
حتى شهر أبريل من العام 2013، ثمانية أدوية لتعديل مسار التصلب المتعدد تم السماح باستخدامها من قبل الجهات التنظيمية للعديد من الدول، من ضمنها إدارة الغذاء والدواء الأمريكية، وكالة الأدوية الأوروبية ووزارة الصحة اليابانية. الأدوية التي تم السماح بها مع أسماء علاماتها التجارية هي انترفيرون بيتا-1-أي (افونيكس، ريبف، سينوفيكس، راسيجن), انترفيرون بيتا-1-بي (بيتاسيرون)، جلاتيرامر اسيتيت (كوباكسون)، ميتوكسانترون (نوفانترون)، ناتاليزوماب (تيسابري)، فينغوليمود (جيلينيا)، تيريفلونومايد (أوباجيو)، ديميثيل فيوماريت (بي جي 12، تيكفيديرا).
وصف الأدوية
في عام 1993 كان انترفيرون بيتا-1-بي أول الأدوية التي سُمح باستخدامها لعلاج التصلب المتعدد، تم بعدها السماح باستخدام انترفيرون بيتا-1-أي وجلاتيرامر اسيتيت. انترفيرون بيتا-1-أي يتم استخدامه عن طريق الحقن مرة أسبوعياً (قالب:حقن عضلي)، أو ثلاث مرات في الأسبوع (الحقن تحت الجلد). أما انترفيرون بيتا-1-بي يتم حقنه تحت الجلد مرة كل يومين. انترفيرون بيتا تعمل على موازنة العوامل المسببة للالتهاب والعوامل المضادة للالتهاد في المخ، وتقوم على تقليص عدد الخلايا الالتهابية التي تعبر الحاجز الدموي الدماغي. إجمالاً، العلاج باستخدام انترفيرون بيتا يؤدي إلى تقليص التهاب الأعصاب. علاوة على ذلك، تقوم بزيادة إنتاج عامل نمو الأعصاب لتؤدي إلى زيادة نسبة سلامة الأعصاب. جلاتيرامر اسيتيت هو مزيج من مبلمرات عشوائية لأربع أحماض أمينية والتي تتشابه مستضدياً مع بروتين المايلين الأساسي مما يجعلها تتنافس معه على التقدم للخلية التائية. يحقن الجلاتيرامر اسيتيت يومياً تحت الجلد. ميتوكسانترون هو مثبط مناعي يستخدم أيضاً في العلاج الكيميائي لمرضى السرطان والذي تم السماح باستخدامه كعلاج للتصلب المتعدد في عام 2000. أما ناتاليزوماب فهو جسم مضاد وحيد النسيلة والذي تم السماح باستخدامه مبدئياً في العام 2004. يتم استخدام ميتوكسانترون وناتاليزوماب عن طريق الحقن الوريدي، لكن ناتاليزوماب يتم استخدامه مرة كل شهر، أما ميتوكسانترون فيتم استخدامه مرة كل ثلاثة أشهر. في عام 2010، تم السماح باستخدام فينغوليمود وهو معدل لمستقبل سفينجوسين-1-فوسفيت من قبل هيئة الغذاء والدواء ليصبح أول علاج يؤخذ عن طريق الفم. في عام 2012 تبعه تيريفلونومايد، وهو يستخدم لمنع إنتاج البيريميدين ويعيق التفاعل بين الخلية التائية والخلية مقدمة للمستضد. يتم استعمال فينغوليمود وتيريلفونومايد على شكل جرعة واحدة يومياً. في عام 2013، تم السماح باستخدام عقار آخر يستخدم عن طريق الفم وهو ديميثيل فيوماريت أو بي جي 12 (وهو يعتبر نسخة مطورة من حمض الفوماريك، وهو دواء يستخدم حالياً). يتم استخدام ديميثيل فيوماريت مرتين يومياً. في العام 2010, روسيا وأستراليا قامتا بالسماح باستخدام عقار آخر يؤخذ عن طريق الفم وهو كلادريبين. في عام 2011 تم رفض استخدامه من قبل إدارة الغذاء والدواء الأمريكية ووكالة الأدوية الأوروبية نظراً لخوفهم من سلامة استخدام الدواء ومن ناحية فعاليته في المعالجة. أدى هذا الرفض إلى سحب الدواء من الأسواق. معظم هذه العقارات والأدوية مسموح استخدامه في النوع الأول وهو التصلب المتعدد المتصاعد الثانوي (حينما تحدث حالات الاتنكاسية والشفاء بشكل متوالي).
الأعراض الجانبية

الأدوية المحقونة قد تسبب تهيج أو كدمة عند موقع الحقن. الكدمة في الصورة سببها حقنة تحت الجلد .
تهيج في مكان حقن جلاتيرامر اسيتيت .
الانترفيرون والجلاترامر اسيتيت يتوفران على هيئة حقن فقط، وكلاهما يتسبب ببعض الآثار الجلدية في مكان الحقن خاصة مع الحقن تحت الجلد. الآثار الجلدية تختلف بشكل واسع من حيث الظهور الاكلينيكي وقد تشمل الكدمات، الاحمرار، الآلام، الحكة، التهيج، الالتهاب وفي الحالات القصوى قد يسبب نخر الجلد. عادة تظهر هذه العلامات في الشهر الأول من العلاج، وان لم تكن ذات أهمية عالية، فإنها غالباً تنتهي بعد مدة ستة أشهر. عادة لا تحتاج بعض الآثار الجلدية المتوسطة إلى إيقاف العلاج، أما في حالة ظهور نخر جلدي، وهو ما يحدث في 5% من الحالات، فيتم إيقاف العلاج. في بعض الأحيان، بعد مدة طويلة من استخدام العلاج قد يظهر تجويف بسيط في مكان الحقن بسبب تحطم النسيج الدهني وهو ما يعرف بالضمور الشحمي. الانترفيرون، وهي أحد الفئات الفرعية للسيتوكين، يتم تصنيعه في الجسم في حالات المرض، كالانفلونزا، ليساعد على القضاء عليها ومساعد الجسم على الشفاء. الانترفيرون مسؤول عن العديد من الاعراض المصاحبة لعدى الإنفلونزا كالحمي، الألم العضلي، الإعياء والصداع. العديد من المرضى يشتكون من أعراض مشابهة للإنفلونزا بعد أخذ الانترفيرون بيتا بساعات، ولكنها عموماً تتحسن في غضون 24 ساعة بما أنها ترتبط مباشرة بالزيادة المؤقتة للسيتوكين. هذه الأعراض عامة ما تبدأ في الاختفاء بعد ثلاثة أشهر من العلاج ولكن يمكن علاجها ببعض الأدوية البسيطة مثل مضادات الالتهابات اللاستيروايدية كالإيبوبروفين والتي غالباً ما تقلل الحمي والألم. أحد الأعراض الأخرى والشائعة لاستخدام انترفيرون بيتا هو التدهور الوظيفي لبعض الأعراض الموجودة سابقاً نتيجة التصلب المتعدد. يشابه هذا التدهور ما يحدث مع مرضى التصلب المتعدد حين تدهور أعراضهم بسبب الحمي أو التوتر (وهي ما تسمى بظاهرة اوتوف). غالباً ما تكون هذه التدهورات للأعراض خلال الفترة الأولى من العلاج ولمدة 24 ساعة إلى عدة أيام بعد الحقن. يعتبر التشنج أحد أكثر أعراض التصلب المتعدد والتي تتدهور مع استخدام انترفيرون بيتا. بالإضافة إلى ذلك، انترفيرون بيتا قد تسبب قلة كريات الدم البيضاء، قلة اللمفاويات، قلة العدلات كما أنها قد تؤثر على وظائف الكبد. عادة ما تكون هذه التغيرات غير خطيرة وبالإمكان عكسها واسترجاع النتائج الطبيعة في حالة تقليل العلاج أو ايقافه. مع ذلك، من المستحسن أن يتم متابعة تحليل الدم وتحليل وظائف الكبد لكل المرضى الذين يستخدمون انترفيرون بيتا وذلك لضمان سلامة المريض. غالباً، جلاتيرامر اسيتيت لا يسبب مشاكل أو مضاعفات مع المرضى. لكن بعض المشاكل الشائعة مع استخدام جلاتيرامر اسيتيت مرتبطة بالجلد. غالباً ما تكون مشاكل مرتبطة بالحقن وتبدأ على شكل بيغ، ثقل في الصدر، خفقان قلبي، ضيق في التنفس والقلق غالباً لا تزيد عن ثلاث دقائق ولا تحتاج إلى العلاج أو التحكم بها. العلاج باستخدام الميتوكسانترون يصاحبه تثبيط للمناعة بالإضافة إلى التسمم الكبدي. على كل حال، فإن أخطر الأعراض الجانبية هو التسمم القلبي والذي يرتبط بالجرعة المأخوذة. لذلك، يجب استخدامه بحذر شديد ومراقبة النتائج بشكل مستمر. من الأمور التي تقلل من احتمالية التعرض للتسمم هو إجراء تخطيط صدى القلب واجراء تحليل دموي شامل قبل البدء في العلاج لتحديد ما إذا كان العلاج مناسباً للمريض أم أنه خطير. ينصح بإيقاف العلاج باستخدام ميتوكسانترون حال وجود علامات لتلف قلبي، عدوى أو اختلال وظيفي للكبد. تظهر اختلالات وظيفية في القلب (خلل انقباضي بشكل رئيسي) في 10% من المرضى، بينما يظهر ابيضاض الدم (اللوكيميا) في 0.8% من المرضى. بعد فترة قصيرة من السماح باستخدام ناتاليزوماب، تم سحبه من الأسواق عن طريق الشركة المصنعة لارتباطه بثلاثة حالات عصبية نادرة تسمى اعتلال بيضاء الدماغ العديد البؤر المترقي. هذه الحالة العصبية النادرة هي من أنواع العدوى الانتهازية التي تتسبب في تطور الأعراض العصبية بسبب تناسخ فيروس جون كونينغهام في الخلايا الدبقية في الدماغ. في جميع الحالات الثلاثة، تم استخدام ناتاليزوماب مع انترفيرون بيتا-1-أي. بعد مراجعة السلامة الدوائية لنتاليزوماب، تم إعادة الدواء في 2006 إلى السوق، لكن يتم استخدامه كعلاج وحيد للتصلب المتعدد وتحت برنامج خاص للوصف الدوائي. في شهر مايو من عام 2011، تم الإبلاغ عن حدوث اعتلال الدماغ العديد البؤر المترقي عند 130 مريض ممن استخدموا ناتاليزوماب لأكثر من عام. لم يستعمل أحد من هؤلاء المرضى علاجاً آخر مع ناتاليزوماب، ولكن في حالة وجود تاريخ لاستخدام علاج آخرقبل ناتاليزوماب قد يرفع احتمالية الإصابة باعتلال الدماغ العديد البؤر المترقي لثلاث أو أربع مرات. تقدر احتمالية الاصابة باعتلال الدماغ العديد البؤر المترقي باصابة ونصف من كل ألف حالة يستخدم فيها ناتاليزوماب. حوالي 20% من مرضى التصلب المتعدد ممن يصابون باعتلال الدماغ العديد البؤر المترقي يتوفون، أما البقية فانهم في الغالب يصابون باعاقات كبيرة. ظهرت خلال مرحة التجارب السريرية لفينغوليمود الآثار الجانبية التي يسببها ومنها ارتفاع ضغط الدم، بطء القلب، وذمات بقعية، زيادة في انزيمات الكبد أو نقصان عدد الخلايا اللمفاوية. يعتبر تيريفلونومايد من أكثر الأدوية أماناً. مع ذلك، فقد تم الإبلاغ عن حدوث حالات من فشل الكبد واعتلال بيضاء الدماغ العديد البؤر المترقي. كما يعتبر تيريفلونومايد شديد الخطورة على نمو الأجنة. أشارت التجارب السريرية أن من أكثر الأعراض الجانبية حدوثاً وشيوعاً عند استخدام ديميثل فيوماريت البيغ وبعض المشاكل المتعلقة بالجهاز الهضمي. هذه الأعراض كانت طفيفة في الغالب وأكثر شيوعاً في الشهر الأول من العلاج. أحد المشاكل عند استخدام ديميثل فيوماريت هو حدوث نقص في عدد كريات الدم البيضاء، لذا يجب مراقبتها مستوياتها باستمرار. على الرغم من أن ديميثل فيوماريت يسبب نقص في عدد كريات الدم البيضاء فإنه لم تسجل حالات عدوى انتهازية عند المرضى. من ناحية أخرى، يستخدم حمض الفيوماريك في علاج الصدفية، وهو أحد أمراض المناعة الذاتية، ويوجد بيانات تؤكد سلامة استخدامه على المدى الطويل، حيث تم استخدامه لمدة أكثر من 14 عاماً دون حدوث مضاعفات ثانوية.
المتلازمة السريرية المعزولة
أول العلامات لحالة الانتكاسة والشفاء هي المتلازمة السريرية المعزولة وتعنى بذلك، ظهور حالة هجوم مرضي واحدة مع وجود علامة واحدة للمرض. في هذه الحالة، يكون الهجوم ما دون الحاد ويشير إلى احتمالية بدء زوال طبقة المايلين ولكن لا يوجد علامات كافية لإكمال التشخيص بالتصلب المتعدد. العلاج باستخدام إنترفيرون أو جلاتيرامر اسيتيت بعد هذا الهجوم المبدئي للمرض قد يقلل من نسبة تطوره إلى التصلب المتعدد.
التصلب المتعدد الانتكاسي الشفائي
الأدوية فعالة بشكل متواضع في تقليل عدد النوبات في حالة التصلب المتعدد الانتكاسي الشفائي، كما أنها قليلة الفعالية من ناحية تقليل تراكم جروح المخ والتي عادة ما تقاس باستخدام جهاز الرنين المغناطيسي المحسن بعنصر الغادولينيوم. تقريباً، يتساوى تأثير كل من الانترفيرون والجلاتيرامر اسيتيت بحيث يقللان من الانتكاسات بنسبة 30%. يتميز كل من الانترفيرون والجلاتيرامر اسيتيت بأنها من أكثر الأدوية أماناً مما يجعلهما أول الأدوية اختياراً. مع ذلك، عدد من مرضى التصلب المتعدد لا يستجيبون للعلاج بالانترفيرون والجلاتيرامر اسيتيت، فمن المعروف أن 30% منهم لا يستجيبون للعلاج بانترفيرون بيتا. من العوامل المؤدية لعدم الاستجابة للعلاج عند بعض المرضى هو وجود الاجسام المضادة المستعدلة لانترفيرون بيتا. العلاج باستخدام انترفيرون، وخصوصاً انترفيرون بيتا-1-بي، يساعد على إنتاج الأجسام المضادة المستعدلة في الأشهر الستة الثانية من بدأ العلاج في 5% إلى 30% من المرضى. علاوة على ذلك، بعض المرضى الذين يعانون من أحد الأنواع الخاصة النشطة للتصلب المتعدد الانتكاسي الشفائي، يسمى بالتصلب المتعدد سريع التفاقم، لا يحملون أي استجابة لمعدلات المناعة ولذلك يتم علاجهم بميتوكسانترون أو ناتاليزوماب. يتعبر ناتاليزوماب وميتوكسانترون من الأدوية شديدة الفعالية من ناحية تقليل عدد الانتكاسات وإيقاف تطور الإعاقات. مع ذلك، يرتبط استخدامهما بأعراض جانبية خطيرة مما جعلهما ثانياً من الاختيار. ناتاليزوماب يحمل فعالية بنسبة أكبر من 70%. علاوة على ذلك، يعتبر ميتوكسانترون مفيد من ناحية تقليل النوبات والاعاقات، ولكن لا يتم استعماله على المدى الطويل لكونه يؤدي لتسمم حاد للقلب. حالياً، لا يوجد دلائل إرشادية لاستخدام الأدوية المعدلة للمرض والتي تؤخذ عن طريق الفم لحداثة تطويرها. بينما يعتقد البعض أنها من الممكن أن تقلل من استخدام الادوية الأولى من ناحية الاختيار، تظل سلامة استخدام الانترفيرون والجلاتيرامر اسيتيت على المدى الطويل أحد العوائق لهذا التحول. في الوقت الراهن، يستحسن استخدام الأدوية التي تؤخذ عن طريق الفم في حالة المرضى لم يستخدموا الأدوية الأخرى نظراً لخوفهم من الإبر أو في حالة عدم فعالية الانترفيرون والجلاتيرامر اسيتيت. كما يمكن استخدامهم مع المرضى الذين يستعملون ناتاليزوماب ووجد لديهم إنتاج للاجسام المضادة لفيروس جون كونينغهام مما قد يرفع احتمالية اصابتهم باعتلال بيضاء الدماغ العديد البؤر المترقي. يعتبر ديميثيل فيوماريت من الأكثر الأدوية الواعدة والتي تؤخذ عن طريق الفم لوفرة المعلومات الموجودة عنه، حيث تم استخدامه لفترة طويلة في علاج الصدفية. من خلال المعلومات المتوفرة عن ديميثيل فيوماريت، يتضح أنه من أكثر الأدوية أمناً. بينما نحتاج إلى عدة دراسات للأعراض التي تسببها الأدوية على المدى الطويل، وخاصة للأدوية الحديثة، يوجد العديد من المعلومات عن الأعراض التي يسببها الانترفيرون والجلاتيرامر اسيتيت. تشير الدراسات إلى أن البدء مبكراً في العلاج الطويل ترتبط بمستوى آمان أكثر بالإضافة لكونها مرتبطة بنتائج أفضل. حتى مع الاستخدام المناسب للأدوية، يعاني العديد من مرضى التصلب المتعدد الانتكاسي الشفائي من بعض النوبات والإعاقات على مستويات مختلفة.
التصلب المتعدد المتصاعد الثانوي والتصلب المتعدد المتصاعد الانتكاسي

التركيب الكيميائي للميتوكسانترون
يعتبر علاج الحالات المتقدمة من التصلب المتعدد أصعب من علاج التصلب المتعدد الانتكاسي الشفائي. تم تجربة العديد من الأدوية لمحاولة إبطاء عملية تطور المرض في هذه الحالات، ولكن النتائج كانت في أفضلها متوسطة الفعالية. أظهر الميتوكسانترون فعالية إيجابية عند استخدامه مع مرضى التصلب المتعدد المتصاعد الثانوي والتصلب المتعدد المتصاعد الانتكاسي. يعتبر الميتوكسانترون متواضع الفعالية في تقليل تطور المرض وفي تقليل النوبات الانتكاسية في حالة المرضى الذين يستخدمونه لمدة قصيرة. في عام 2007، كان الميتوكسانترون العلاج الوحيد المسموح باستخدامه في الولايات المتحدة مع مرضى التصلب المتعدد المتصاعد الثانوي والمتصاعد الانتكاسي. غير أن الميتوكسانترون تسبب بحالات تسمم القلب المعتمدة على الجرعة، مما أدى إلى إيقاف استخدامه على المدى الطويل. أما في أوروبا، فإنه لا يسمح باستخدام الميتوكسانترون في علاج التصلب المتعدد. في الجانب الآخر، أظهر ناتاليزوماب فعالية جيدة مما أدى إلى السماح باستخدامه في علاج التصلب المتعدد المتصاعد الثانوي المصحوب بانتكاسات. أكدت بعض الدراسات التي أجريت على استخدام انترفيرون بيتا-1-بي في حالات التصلب المتعدد المتصاعد الثانوي والمتصاعد الانتكاسي أنه لا يؤدي إلى إبطاء تطور المرض، مع أنه تم تأكيد فعاليته في تقليل عدد النوبات الانتكاسية.
التصلب المتعدد المتصاعد الأساسي
يواجه علاج التصلب المتعدد المتصاعد الأساسي العديد من المشاكل، حيث أن العديد من المرضى لا يستيجبون للعلاجات المتوفرة، إضافة إلى عدم وجود علاج محدد لهذا النوع من المرض. أجريت العديد من الدراسات حول تأثير العديد من الأدوية على مسار هذا النوع من التصلب المتعدد، إلا أنه لم تنتج أحد الأدوية نتيجة إيجابية. من الأدوية التي تم دراستها هي انترفيرون بيتا، ميتوكسانترون، جلاتيرامر اسيتيت وريلوزول. بالإضافة إلى أنه تم إدخال بعض مرضى التصلب المتعدد المتصاعد الأساسي في العديد من الاختبارات التجريبية لبعض الادوية ومنها آزاثيوبرين، ميثوتركسيت، جسيم مضاد وريدي، سيكلوفوسفاميد وزراعة نخاع العظم.
التحكم بتأثيرات المرض
الأدوية المعدلة لمسار المرض تتحكم فقط في عملية إبطاء المرض ولكنها لا توقفه. عادة، عند تطور مرض التصلب المتعدد فإن العلامات والأعراض تتطور معه أيضاً. يصاحب المرض العديد من الأعراض المتنوعة ووالاعتلالات الوظيفية المختلفة والتي بدورها تؤدي إلى تدهور مستمر للمريض بالإضافة إلى بعض الإعاقات. لذلك، فإن التحكم بهذه الاعتلالات وعلاجها أمر مهم جداً. استخدام الأدوية وطرق التأهيل العصبي ساعدت على تخفيف عبء بعض الأعراض المرضية مع أن كلاهما، أي الأدوية والتأهيل العصبي، لم يؤدِ إلى إبطاء سير المرض. عموماً، بعض الأعراض التي يسببها التصلب المتعدد لا يوجد طرق لعلاجها أو التحكم بها حالياً.
التأهيل العصبي
للمزيد من المعلومات:التصلب اللويحي و العلاج الوظيفي
على الرغم من وجود عدد قليل نسبياً من الأبحاث حول إعادة التأهيل لمرضى التصلب المتعدد، إلا أن الفعالية المستفادة من إعادة التأهيل العصبي والتي تؤدى من قبل فريق متخصص كانت تقابل بعدد من الأمراض والمشاكل في الأجهزة الحيوية الأخرى، فمثلاً، قد تسبب السكتة الدماغية أو إصابات الرأس. عموماً، كما في حال جميع المرضى الذين يعانون من نقص في الوظائف العصبية، يجب استخدام طرق من عدة مجالات متخصصة لهدف تخفيف تطور الإعاقات بل وإيقافها أيضاً. المشكلة في عدم القدرة على تكوين فريق متكامل ومتخصص لعلاج هذه الحالات يكمن في أن مرضى التصلب المتعدد يحتاجون المساعدة من كثير من التخصصات الطبية المختلفة وعلى مراحل متعددة. أخصائيوا المخ والأعصاب هم المسؤولون بشكل رئيسي عن التشخيص والعلاج والتحكم في جميع الحالات المتفاقمة. أخصائيوا الأمراض والحالات النفسية هم غالباً المسؤولين عن إعادة التأهيل الشاملة لمرضى التصلب المتعدد. يمكن إضافة بعض العلاجات والتخصصات المساعدة كالعلاج الفيزيائي، أخصائيي علم أمراض النطق واللغة وأخصائيي العلاج الوظيفي لعلاج والتحكم ببعض الأعراض للإبقاء على نوعية حياة أفضل. لعلاج بعض أعراض الاضطرابات العصبية النفسية كالضغوطات العاطفية والاكتئاب، يجب إشراك بعض الأخصائيين من الصحة النفسية كأخصائيي العلاج النفسي، علماء النفس والأطباء النفسيين، بينما يعمل أخصائيوا علم الطب العصبي النفسي على تقييم وعلاج الاعتلالات المعرفية. أظهرت طرق العلاج باستخدام التخصصات المختلفة فعالية في زيادة مستويات النشاط والمشاركة في التصلب المتعدد. نظراً لقلة الدراسات العشوائية، فإنه يوجد أدلة محدودة على الفعالية العامة للعلاج باستخدام تخصص واحد، ولكن يوجود أدلة جيدة على فعالية العلاج باستخدام تخصص محدد كالتدريب، العلاج النفسي، وخصوصاً العلاج السلوكي المعرفي، كما أن تعليمات الحفاظ على الطاقة مفيدة أيضاً. يُظهر التدخل العلاجي النفسي فعالية عالية في علاج قالب:اكتئاب ، بينما لا يوجد أدلة على فعالية بعض التخصصات الأخرى في علاج الاكتئاب كعلاج الاعتلال المعرفي أو الإرشاد المهني. من الصعب التحديد بدقة التخصص التأهيلي الأكثر فائدة في علاج مرضى التصلب المتعدد، لأن العلاجات التأهيلية مصممة لتناسب كل مريض على حدة. في ما يتعلق بالرضى العام لمرضى التصلب المتعدد، العلاج الفيزيائي (الطبيعي) للتدريب على المشي والحركة قد يقود إلى زيادة مشاركة ومساهمة مرضى التصلب المتعدد في المجتمع من خلال تقليل التعب الحاصل جراء المشي أو عند أداء أنشطة الحياة اليومية. معظم التدريب على المشي يتم على الأرض كأراضي الصالات الرياضية أو الأرض غير المتساوية، أجهزة المشي وفي حالات أقل، يتم استخدام الأجهزة المعدة روبوتياً. أجهزة المشي المعدة بالتقنية الروبوتية تعد أحد أفضل الحلول المستخدمة مع مرضى التصلب المتعدد الذين يعانون من اعتلالات شديدة في المشي. على النقيض، فإن التدريب على المشي والذي يتم على الأرض يكون شديد الفعالية والنجاح مع المرضى الذين يعانون من اعتلالات خفيفة في المشي. المداواة باستخدام الطرق الخيلية مثل ركوب الخيل العلاجي والعلاج باستخدام الخيل هي أحد العلاجات التي قد تؤثر بشكل ايجابي على المشي والتوازن ونوعية الحياة لدى مرضى التصلب المتعدد. في السابق، كان ينصح مرضى التصلب المتعدد بعدم المشاركة في الأنشطة التي تتطلب حركة جسدية لما لها من أثر في زيادة تدهور الأعراض. في الوقت الحالي، يسمح لمرضى التصلب المتعدد بالمشاركة في الأنشطة الجسدية، تحت إشراف شخص متخصص وخبير، حيث وُجد أنها آمنة بل وقد تفيد مرضى التصلب المتعدد. تشير بعض الدراسات إلى أن الأنشطة الجسدية تلعب دوراً هاماً في تحسين قوة العضلات، الحركة، المزاج النفسي، صحة الجهاز الهضمي، التكيف العام ونوعية الحياة. اعتماداً على المريض، قد تتخلل بعض الأنشطة تدريب المقاومة، المشي، السباحة، اليوغا، تاي تشي وتمارين أخرى. يعتبر تحديد التمرين المناسب والآمن للمريض أحد الصعوبات والتحديات التي يجب الحذر عندها، حيث يجب أن يتم اختيار التمارين لكل مريض على حدة لتناسبه ولالتزام كافة وسائل السلامة والابتعاد عن ما قد يؤذي المريض. خلال التمارين، لوحظ زيادة ظهور الأعراض نظراً لزيادة درجة حرارة الجسم الرئيسية، سبب ذلك هو اختلاف درجة حرارة الجسم والساعة البيولوجية بين شخص وآخرخلال اليوم. السبب الآخر وهو زيادة التعرض لدرجات حرارة عالية كالحمام الدافئ، الاستحمام الدافئ والتسفع. لذلك، يجب الحذر من ارتفاع درجة حرارة جسم المرضى خلال إجراء التمارين. يوجد بعض الأدلة التي تؤكد فعالية بعض طرق التبريد في زيادة وقت التمرين دون ارتفاع الحرارة ومنها الاستحمام البارد، غطس الأطراف بالماء البارد، استخدام كمادات الثلج وشرب السوائل الباردة. هذه الطرق والاستراتيجيات فعالية في تقليل درجة حرارة الجسم بعد التمرين، قبل التمرين أو قبل التعرض لدرجات حرارة عالية. التفاعل الذي يحدث عند ارتفاع درجة حرارة الجسم وحركة ازالة المايلين الناتجة من المرض تؤدي إلى اعتراض وايقاف عابر (وقتي) للتوصيل العصبي والتي تسبب إلى إضعاف بعض الوظائف الجسدية والمعرفية لفترة مؤقتة. هذا التفاعل يؤدي إلى تقليص نسبة الأمان والأداء لأنشطة الحياة اليومية، ولكن يوجد بعض الطرق المجدية لإيقاف ومنع هذه النتائج. بعض الطرق السلوكية التي تقلل من التعرض للحرارة الزائدة تتضمن إجراء الأنشطة الجسدية في الهواء الطلق في حالة الجو البارد أو تركيب جهاز تكييف في مكان إجراء التمارين.
علاج أعراض مرض التصلب المتعدد
يسبب مرض التصلب المتعدد العديد من الأعراض التي تشمل تغير الإحساس (تغير الإحساس)، ضعف عضلي، تشنج عضلي غير طبيعي، ضعف حركي، صعوبة في التناسق والتوازن، مشاكل في النطق واللغة (تعرف بعسر التلفظ)، صعوبة في ابتلاع الطعم (عسر البلع)، مشاكل في النظر (رأرأة، التهاب العصب البصري، ازدواج الرؤية)، إعياء ومتلازمة الألم الشديد أو المزمن، مشاكل في الأمعاء والمثانة، ضعف معرفي أو عاطفي (غالباً الاكتئاب). في نفس الوقت، يوجد لكل عرض مرضي أكثر من خيار علاجي واحد. لذا، فإنه يجب أن تكون عملية العلاج فردية لكل مريض على حدة واعتماداً على المريض نفسه وعلى الطبيب. المثانة: ظهور أعراض مرضية في الجهاز البولي هو أحد الأمور الشائعة لدى مرضى التصلب المتعدد. تختلف الأدوية المتاحة لعلاج مشاكل المثانة بناء على مصدر الألم أو نوع الخلل الوظيفي، ولكن يمكن تقسيمها بشكل عام إلى أدوية التحكم بالمثانة وسلس البول، وأدوية علاج عدوى الجهاز البولي. للتحكم في المثانة، يوجد عدد من الأدوية المتاحة ومنها ديسموبريسين لعلاج البوال الليلي ومضادات الكولين كاوكسيبيوتينين وتولتيرودين الذي يستخدم لعلاج حالات الالحاح البولي. يوجد عدد من الطرق الأخرى للتحكم بالمثانة والتي تتم بدون استخدام الأدوية وتشمل تدريب عصلات قاع الحوض، التحفيز، الفرزجة، تدريب المثانة، تغيير بعض العادات اليومية كاللباس، استعمال أداة جمع البول الخارجية للرجال ومنشفة حبس البول للنساء، وفي بعض الأحيان قسطرة تصريف البول المتقطعة (أي تستخدم لفترات متقطعة وليس بشكل دائم). أما فيما يخص القسطرة البولية على المدى الطويل فإنها ترتبط بعدوى الجهاز البولي، ولذلك يفضل دوماً تجنب استخدامها متى ما أمكن. بعض هذه الأمور المذكورة لم تذكر بشكل محدد في الدراسات التي تخص التصلب المتعدد، ولكنها من الأمور العامة المستحسن اتباعها من قبل الذين يعانون من خلل في المثانة سببه أحد الأمراض العصبية.
الأمعاء: تؤثر الأعراض المعوية على 70% من مرضى التصلب المتعدد، وقرابة 50% من المرضى يعانون من الإمساك وحوالي 30% من سلس البراز. من أكثر الأسباب المؤدية للمشاكل المعوية هي قلة حركة الأمعاء أو الضعف في التحكم العصبي بعملية التبرز. يرتبط الضعف في التحكم العصبي بالتبرز بعدم القدرة على التحرك أو كسبب ثانوي لأحد الأدوية المستخدمة في علاج التصلب المتعدد. يمكن التحكم في المشاكل والآلام المرتبطة بعملية التبرز عن طريق تغيير الوجبات الغذائية بجعلها تشمل زيادة في في السوائل، ملينات البراز، التحاميل والحقن الشرجية في حالة أن الحلول الغذائية لم تنفع في التحكم في المشكلة.
المعرفة والعاطفة: الأعراض العصبية النفسية هي من العلامات الشائعة التي تصاحب مرض التصلب المتعدد. يظهر لدى 80% من مرضى التصلب المتعدد أعراض الاكتئاب والقلق. من الشائع أيضاً التوتر العصبي والذي يؤدي إلى بكاء لا يمكن التحكم به. هذه الأعراض يمكن التحكم بها عن طريق استخدام مضادات الاكتئاب والعلاج السلوكي المعرفي، مع ذلك، فإنه لا يوجد دراسات ذات جودة عالية لاثبات فعاليتها علمياً. فعلى سبيل المثال، في حالة مضادات الاكتئاب ودورها في الاكتئاب، فإنه تم اعتبار دراستان جديرتان بالاهتمام في عام 2011 من قبل منظمة كوكرن، وأوضحت الدراستان بعض التوجه لفعالية الأدوية. تشمل بعض الأعراض العصبية النفسية النشوة ومنع التثبيط الذاتي. في العشرين عام الماضية، كانت ولازالت الاعتلالات المعرفية من الأعراض المعتادة للتصلب المتعدد حتى بعد استخدام الأدوية المعدلة لمسار المرض. حتى مع اعتبار ان المرض هو المسبب الأساسي للاعتلال المعرفي، بعض العناصر تلعب دوراً هاماً كالأدوية، الانتكاسات والاكتئاب، ولذا يجب الاهتمام بالتقييم الصحيح للمشكلة والعناصر التي تسببها. في ما يخص العجز الأساسي، تشير البيانات إلى أن استعمال ال-امفيتامين وميثيلفينيديت مفيد، بينما ميمانتين ومثبطات الكولينستريز كالدونيبيزل (يستخدم بشكل شائع في علاج مرض الزهايمر)، تعتبر غير مفيدة أو فعالة في حل الاعتلالات المعرفية. من الطرق المطبقة أيضاً هي إعادة التأهيل المعرفي ولكن يحيط الكثير من الجدل حول فعاليتها. عسر البلع وعسر اللفظ: عسر البلع هي مواجهة صعوبة في الأكل والابتلاع والتي قد تسبب الشّرَقْ أو دخول السوائل إلى الرئة، أما عسر اللفظ فهو اضطراب عصبي في مركز الكلام الحركي يتميز بالضعف في التحكم بالأنظمة والعضلات المسؤولة عن النطق. لعلاج هذه المشاكل، يقوم أخصائيوا علاج النطق واللغة بإعطاء بعض النصائح للمرضى من حيث بعض طرق البلع، استخدام نظام غذائي متماسك، تحسين وتطوير النطق ووضوحه وإمكانية استخدام طرق تواصل بديلة. في حالة عسر البلع الشديدة، يمكن إدخال الغذاء عن طريق الأنبوب الانفي المعوي والذي يوصل الغذاء مباشرة من الأنف إلى المعدة، أو بالإمكان استخدام الانبوب من الجلد إلى المعدة مباشرة عن طريق عمل فتحة في البطن.تعتبر العملية الثانية، مع أنها أكثر تدخلاً، أكثر فعالية على المدى الطويل من الأنبوب الانفي المعوي.
ضعف الانتصاب: ضعف الانتصاب أو العنة هو أحد الاعراض الشائعة عند المرضى من الذكور. توجد بعض الأدلة التي تشير إلى أن سيلدينافيل قد يكون علاجاً فعالاً.
الإعياء: الإعياء هو أيضاً من أكثر الأعراض شيوعاً لدى مرضى التصلب المتعدد، ويحمل الإعياء علاقة وارتباط كبيرين بالاكتئاب. غالباً، عندما يقل الاكتئاب، يقل الإعياء أيضاً. ولذا، فإن تحديد حالة الاكتئاب، ان وجد، مهمة جداً قبل البدء بوضع خطة علاجية للإعياء. يوجد عدد من العناصر الأخرى التي قد تلعب دوراً في زيادة الإعياء كالنوم المتقطع، الألم المزمن، التغذية السيئة، وحتى بعض الأدوية قد تساهم في زيادة الإعياء، ولذلك يجب أن يحرص الأطباء والممارسين الصحيين على التعرف على هذه الأدوية. يوجد عدد من الأدوية التي درس استخدامها لحل مشكلة الإعياء عند مرضى التصلب المتعدد مثل امانتادين وبيمولين (وهو منشط نفسي يستخدم في علاج قصور الانتباه وفرط الحركة ولعلاج التغفيق) ومودافينيل، كما يتم استعمال التدخل النفسي لحفظ الطاقة، ولكن جميعاً لا تؤثر بشكل كبير على المرضى. لذلك، يعتبر الإعياء أحد أصعب الأعراض علاجاً، ولا يوجد له أدوية مستحسنة.
الألم: ينتج الألم الحاد لدى مرضى التصلب المتعدد بشكل رئيسي من التهاب العصب البصري (والذي يتم علاجه بالكورتيزون)، ألم عصب ثلاثي التوائم، علامة ليرميت وخلل الحس. الألم ما تحت الحاد غالباً ما يكون بسبب المرض وقد يكون بسبب البقاء طويلاً على نفس وضعية الجسم، احتباس البول والتهاب تقرح الجلد. لذلك، يكون علاج الألم بناء على السبب. الألم المزمن شائع جداً بين مرضى التصلب المتعدد وهو من أصعب الآلام معالجة لكونه بسبب خلل الحس غالباً. الألم الحاد هو غالباً من نتائج ألم عصب ثلاثي التوائم، وغالباً يتم علاجه بنجاح باستخدام مضادات الاختلاج كالكاربامازيبين أو الفينيتوين. يستيجب كلاً من علامة ليرميت وخلل الحس للعلاج باستخدام كاربامازيبين، كلونازيبام وأميتربتيلين. يسمح باستخدام ساتيفيكس لعلاج الآلام المصاحبة للتصلب المتعدد في عدد من الدول، ولكن لكونه مشتق من نبات القنب، لا يسمح باستخدامه في عدد من الدول الأخرى كالولايات المتحدة الأمريكية. في الوقت الراهن، يتم دراسة استخدام ساتيفيكس في علاج بعض الأعراض الأخرى كالتشنج، وقد أظهر الدواء فعالية وسلامة عالية في الاستخدام على المدى الطويل.
التشنج: يتصف التشنج بزيادة صلابة وبطء حركة الأطراف، اتخاذ بعض الوضعيات الجسدية، علاقة مباشرة مع ضعف قوة العضلات الارادية، تقلص لا إرادي مؤلم للأطراف. يوجد بعض الحلول المستخدمة كالعلاج الفيزيائي (الطبيعي)، بحيث يستخدم المعالج الطرق المختلفة كتمارين الإطالة السالبة لمنع حدوث التقفع (وهو قصر طول أو حجم العضلة بشكل دائم). الدراسات التي تجرى على ساتيفيكس أظهرت نتائج مشجعة لتحسن التشنج. يوجد بعض الأدلة، ولو أنها محدودة، على الفعالية الاكلينيكية لباكلوفين، دانترولين، ديازيبام وتيزانيدين. في الحالات شديدة التعقيد، يمكن استخدام بيكلوفين عن طريق الحقن داخل القراب. يوجد أيضاَ عدد من الطرق التلطيفية كالجبيرة، مثبتات الأطراف والكراسي المعدلة.
الرؤية: يوجد العديد من الأدوية وأنظمة الرؤية التعويضية والنظارات الطبية المزودة بالمواشير لتحسين أعراض الرأرأة وازدواجية النظر. يمكن أيضاً تطبيق العمليات الجراحية في بعض الحالات.
المشي: في الولايات المتحدة، تم السماح باستخدام امبيرا (وهو مجموعة واسعة من محصرات قنوات البوتاسيوم) في علاج مصاعب المشي عند مرضى التصلب المتعدد. مع ارتفاع سعره (حيث يبلغ تكلفته أكثر من 1000 دولار شهرياً)، إلا أن الامبيرا أظهر فعالية عالية في زيادة سرعة المشي.
للأسف، تظل هناك بعض الأعراض التي لا يوجد لها علاجات ثابتة كالرنح (أو عدم تناسق الحركات العضلية الادراية)، الرعاش وفقدان الإحساس.
علاجات
تحت التطوير 
التركيب الكيمائي لأليمتوزوماب
تتوجه الأبحاث العلاجية للتصلب المتعدد نحو الاستقصاء عن الطبيعة الإمراضية والتغايرية للتصلب المتعدد ومنها أبحاث حول أدوية فعالة ومريحة وقابلة للتطبيق في علاج التصلب المتعدد الانتكاسي الشفائي، تطوير علاجات للتصلب المتعدد التصاعدي، استراتيجيات حفظية عصبية، وأبحاث حول طرق علاجية أكثر فعالية للأعراض المصاحبة للتصلب المتعدد. خلال العقد الماضي، تم إجراء العديد من البحوث الجيدة والتي أدت إلى تحسين مستوى الفعالية للأدوية الفموية. يعتقد أن هذه الأدوية ستكون الأكثر استخداماً بين مرضى التصلب المتعدد على حساب الأدوية السابقة. حالياً، يوجد العديد من الأدوية الفموية تحت الدراسات. في شهر اوجست من عام 2012، تم الإعلان عن دواء لاكوينيمود والذي لا يزال في المرحلة الثالثة من الدراسات. بشكل مشابه، تجري العديد من الدراسات لتحسين فعالية الأدوية الموجودة مسبقاً ولتسهيل استخدامها عن طريق استعمال طرق دراسية جديدة. من أشهر الأمثلة على النوع السابق النسخة الجديدة من انترفيرون بيتا-1-أي والتي تتضمن إضافة بولي ايثيلين جليكول، هذا التعديل يزيد من عمر الدواء في الجسم مما قد يجعله بديلاً للدواء الأصلي (في حال تساوى معه من حيث الفعالية) لغرض تقليل عدد الجرعات. يتوقع أن يتم طلب السماح باستخدام هذا الدواء في عام 2013. تعتبر الأجسام المضادة وحيدة النسيلة (كالناتاليزوماب) أحد أكثر الأدوية التي تثير اهتمام الباحثين. أظهرت الأجسام المضادة وحيدة النسيلة كأليمتوزوماب، داكليزوماب وسي دي 20 (مثل ريتوكسيماب، اوكريلزوماب وأوفاتوموماب) بعض الفعالية والفائدة مع مرضى التصلب المتعدد ولا تزال تحت الدراسات للتطبيق على المرضى. ومع ذلك، فقد أظهرت الدراسات أن هذه العلاجات قد يصاحبها ظهور بعض التفاعلات الخطيرة ومن أهمها العدوى الانتهازية. ومن الدراسات المرتبطة بهذا النوع من العلاجات هو ما ظهر حول تطوير فحص لكشف الأجسام المضادة لفيروس جون كونينغهام، وقد يساعد هذا الفحص في تحديد المرضى تحت خطر الإصابة ببيضاء الدماغ العديد البؤر المترقي عند استخدامهم لناتاليزوماب. في حين يعتقد أن الأجسام المضادة وحيدة النسيلة سيكون لها دور في علاج التصلب المتعدد، سيكون هذا الدور بسيطاً وصغيراً نظراً للمخاطر المصاحبة لاستخدامها. أحد الاستراتيجيات المتبعة في الأبحاث الجديدة هي قياس التأثير عند استخدام علاجين في وقت واحد. تأتي هذه الاستراتيجية في العلاج بأكثر من دواء من كون الأدوية المستخدمة في علاج التصلب المتعدد تستهدف طرقاً مختلفة لإيقاف وتخفيف المرض، ولذلك فإن استخدامها ليس حصرياً وإنما بالإمكان الجمع بين أكثر من طريقة لعلاج المرض. ومن جهة أخرى، فإنه من الممكن أن يؤدي أحد الأدوية إلى زيادة تأثير وفعالية دواء آخر. مع ذلك، فإنه يجب الحذر حيث بالإمكان أن تؤدي هذه الطريقة بأن يقلل أحد الأدوية تأثير آخر أو أن يزيد من ضرره مما يؤدي لمشاكل أكبر. مع وجود عدد من الدراسات التي أجريت بهذه الطريقة وباستخدام أكثر من دواء، فإن النتائج لم تكن بالشكل المطلوب أو الذي تطبيق هذه الطريقة في علاج التصلب المتعدد. أخيراً، فيما يخص الدراسات في مجال العلاجات الحافظة العصبية وخاصة التجديدية (كالعلاج بالخلايا الجذعية)، فإنها تعتبر ذات أهمية عالية ولكنها قد تفيد في علاج مستقبلي وليس حالي للتصلب المتعدد. وبشكل مماثل، فإنه لا يوجد أي علاج فعال للنوع المتصاعد من المرض. في الفترة الحالية، سيتم تقييم الكثير من الأدوية الحديثة والأدوية تحت التطوير والدراسة من حيث فعاليتها في علاج التصلب المتعدد المتصاعد الأولي والثانوي، وإذا ظهر أن فعاليتها أعلى من فعالية الأدوية السابقة فإنها غالباً ستستخدم مع المرضى بهذا النوع. في عام 2008، اقترح جراح الأوعية الدموية الإيطالي باولو زامبوني أن مرض التصلب المتعدد يتضمن بعض الخصائص الوعائية والتي أشار لها بالقصور الوريدي المزمن الدماغي، بحيث أن بعض الأوردة في المخ تصبح ضيقة. أكد زامبوني أنه وجد هذه المشكلة الوعائية في جميع مرضى التصلب المتعدد في دراسته وأنه أجرى لهم جميعاً عملية لإزالة هذه المشكلة، وهي ما أسماها الإعلام بعملية التحرير، ومن ثم إدعى أن 73% منهم تحسنوا. لقد شدت هذه الدراسة انتباه الإعلام ومرضى التصلب المتعدد، خاصة في كندا. ولكن ارتفعت بعض الشكوك حول تجربة زامبوني حيث أنها لم تكن عمياء ولم تكن مُحكمة، بالإضافة إلى أن تعريفها للفيزيولوجيا المرضية لم ترتكز على بيانات معروفة. ومن جهة أخرى، فإن الدراسات الأخرى التي أجريت لم تجد علاقة مباشرة أو أنها وجدت دليل بسيطاً على وجود علاقة مباشرة. سبب هذه الأمور اعتراضات جادة على فرضية حدوث التصلب المتعدد جراء الإصابة بالقصور الوريدي المزمن الدماغي. بالإضافة لذلك، فإن «عملية التحرير» واجهت العديد من النقد لكونها قد تُحدث مضاعفات خطيرة ووفيات مع عدم وجود منفعة مثبتة لها. حالياً، فإنه يستحسن عدم استخدام طرق علاجية إلا إذا تأكد فعاليتها بدراسات مُحكمة. تم تسريع الداسات حول القصور الوريدي المزمن الدماغي ولكن الباحثين لم يستطيعوا تأكيد ما إذا كان هو السبب خلف التصلب المتعدد.
أدوية بديلة
أكثر من 50% من مرضى التصلب المتعدد يستخدمون وسائل الطب التكميلي والطب البديل، مع أنهم يختلفون كثيراً حول النوعية المحددة من العلاج المستخدم. الأدلة حول فعالية هذه العلاجات في كثير من الحالات ضعيفة أو غير موجودة. من الأمثلة على العلاجات المستخدمة من قبل بعض المرضى المكملات والأنظمة الغذائية، تقنيات الراحة كاليوغا، التداوي بالأعشاب كالقنب الطبي، التطبيب بالضغط العالي، العدوى الذاتية بالدودة الشصية (تعرف باسم العلاج بالديدان)، العلاج بالعسل، العلاج بالمنعكسات والعلاج بالوخز بالإبر. في ما يخص المرضى الذي يتعاملون بالطب البديل، فهم غالباً من النساء الذين أصيبوا بالمرض لفترة طويلة ويكونون غالباً مصابين بإعاقات كبيرة. غالباً يحمل هؤلاء أيضاً نسبة قليلة من الرضا عن الطب التقليدي.

ليست هناك تعليقات:
إرسال تعليق